生体分子化学研究室(野瀬研究室)のページ
Laboratory of Biomolecular Chemistry
研究内容reSEARCH
生体分子化学研究室の研究内容
当研究室では現在、ペプチド・タンパク質を用いて、主に4種類のテーマで研究を行っています。(1) エラスチン由来ペプチドの構造活性相関
(2) 受容体結合性分子の同定・発見 (特に、内分泌かく乱物質のリスク評価を目的として、計算化学と生物化学の手法を組み合わせて研究を行っています)
(3) 合理的分子設計法を用いた酵素阻害剤の開発
(4) 溶媒摂動法を用いた生体関連分子の分子間相互作用解析
(5) 多量体形成タンパク質の機能制御機構の解明
(1) エラスチン由来ペプチドの構造活性相関
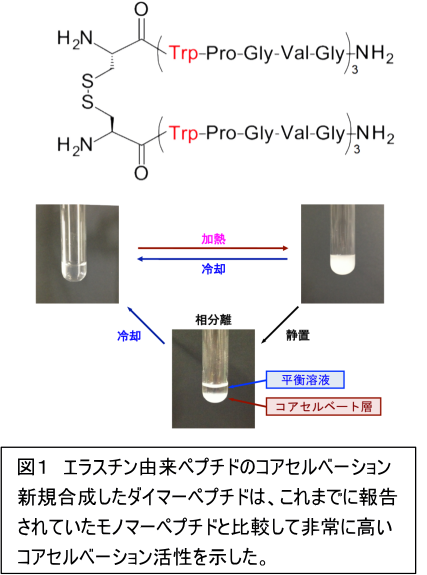 エラスチンは生体内で血管や皮下組織、腱などに多く含まれるタンパク質であり、組織に弾性を与える役割を持っています。エラスチンは「温度を上げると凝集し、下げると再び解離する」という、温度依存的かつ可逆的な自己集合(コアセルベーション)特性を示します。このコアセルベーション特性を応用することで、エラスチンは代用皮膚や人工血管、薬物送達システムの担体などへの応用が期待されています。
エラスチンは生体内で血管や皮下組織、腱などに多く含まれるタンパク質であり、組織に弾性を与える役割を持っています。エラスチンは「温度を上げると凝集し、下げると再び解離する」という、温度依存的かつ可逆的な自己集合(コアセルベーション)特性を示します。このコアセルベーション特性を応用することで、エラスチンは代用皮膚や人工血管、薬物送達システムの担体などへの応用が期待されています。
当研究室では最近、エラスチンの内部のアミノ酸繰り返し配列を模倣した合成ペプチド(Phe-Pro-Gly-Val-Gly)5および(Trp-Pro-Gly-Val-Gly)3のダイマーが非常に高いコアセルベーション能をもつことを明らかにしました。これらのダイマーペプチドは、モノマーと比較して低温・低濃度でコアセルベーションを示したことから、ダイマー化によってペプチドの自己集合能が著しく増強されることが判明しました。この結果に基づき、私たちは生理的条件化でさらに高いコアセルベーション活性を有するペプチドの開発を行っています。
最近の研究成果:
現在、重金属などの環境汚染物質を簡便かつ安全に回収する方法の開発が必要とされています。そこで、金属結合性ペプチド配列と結合した短いエラスチン様ペプチド(ELP)アナログは、容易に合成が可能で、天然アミノ酸のみからなるため環境に優しく、また、金属結合性ペプチド配列(ドメイン、)を任意の標的金属に基づいて選択できることから、金属回収剤として有用であると考えられています。すなわち、ELPの温度依存的な自己組織化により、金属結合性ペプチド配列を負荷されたELPは溶液状態から金属イオンをキレートした粒子へと変化し、沈殿として回収することが可能であると考えられました。本研究では、短いELPである(FPGVG)4のN末端に金属結合配列であるAADAACを導入し検討を行いました。濁度測定において、AADAAC-(FPGVG)4はCd2+やZn2+などの金属イオン存在下で強い自己組織化能を示しました。また、比色分析の結果、AADAAC-(FPGVG)4はCd2+とZn2+を捕捉できることが示されました。さらに、金属イオンに結合したAADAAC-(FPGVG)4は、酸性溶液で処理することにより、金属結合親和性を損なうことなく容易にリサイクルすることが可能でした。本研究により、金属結合配列とELPの融合は、環境負荷の少ない費用対効果の高い重金属捕捉剤を開発するための有用かつ強力な戦略であることが示されました。
Shogo Sumiyoshi, Keitaro Suyama, Daiki Tatsubo, Naoki Tanaka, Keisuke Tomohara, Suguru Taniguchi, Iori Maeda & Takeru Nose. Metal ion scavenging activity
of elastin-like peptide analogues containing a cadmium ion binding sequence.
Sci. Rep., 12, 1861 (2022).
https://doi.org/10.1038/s41598-022-05695-w
本研究は、科学研究費・基盤研究(B) 自己凝集性ペプチドの可逆コアセルベーションによる環境汚染物質吸着システムの開発(JSPS・JP19H0403)、および、科学研究費・挑戦的研究(開拓)天然タンパク質資源の有効活用を目指した機能性マイクロ粒子捕集素材の開発(JSPS・JP 20K20638)による研究成果の一部です。
(2) 受容体結合性分子の同定・発見
「核内受容体」は細胞の核内に存在し、ホルモン等のリガンドが結合することで活性化されてタンパク質の発現を調節する転写因子タンパク質です。一方、環境中に存在する有害な化学物質が核内受容体に結合することにより、本来のホルモンの機能を模倣・阻害して内分泌系に悪影響を及ぼす問題・内分泌攪乱が懸念されています。核内受容体に結合する化学物質の構造を予測することができれば、化学物質による内分泌攪乱リスクを評価するための重要な情報となります。当研究室では、生物化学的な実験と計算化学の手法を組み合わせて、化学物質によるリスク評価の研究を行っています。
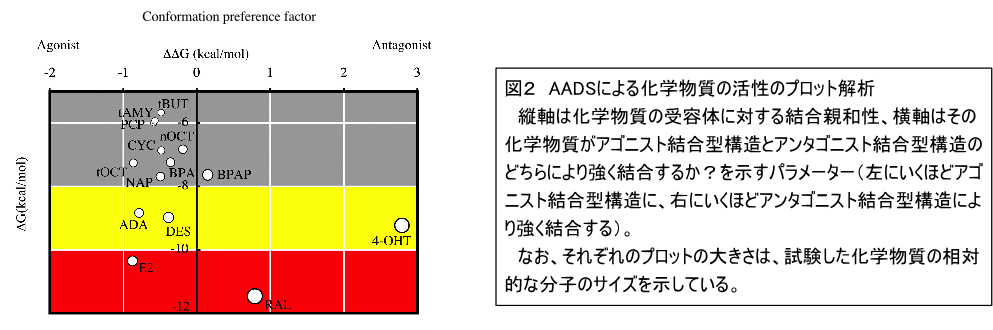
我々は、アゴニスト(受容体を活性化する物質)が結合した受容体、アンタゴニスト(受容体の活性を阻害する物質)が結合した受容体のX線結晶構造をそれぞれ鋳型としてドッキング計算を行い、それぞれの計算結果の結合エネルギーの比較によって化学物質がアゴニスト、アンタゴニストのどちらであるか?を判別する試験法(agonist/antagonist differential-docking screening, AADS)を確立しました。この方法により、計算で化学物質の受容体結合性だけでなく生理活性も予測することが可能となりました。
(3) 合理的分子設計法を用いた酵素阻害剤の開発
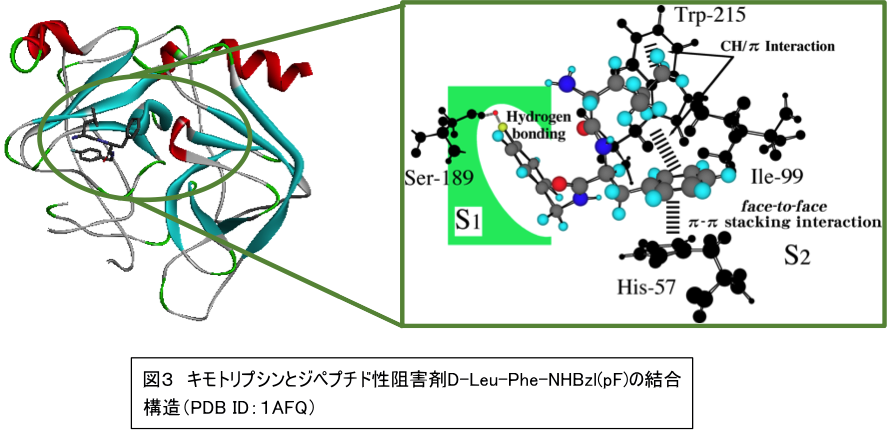
酵素キモトリプシンのジペプチド性阻害剤であるD-Leu-Phe-NHBzl (pF)は、そのフェニル基とキモトリプシンの活性部位に存在するヒスチジンのイミダゾール環の間のπ-πスタッキングを介して酵素活性を阻害します。このπ性の相互作用は、酵素活性の阻害に必須です。
本研究では、新たにデザインした酵素阻害剤の活性を分子力学計算に基づいたドッキング計算によって予測できるか?を検証するため、まずドッキング計算によってジペプチド性阻害剤のN末端にアミノ酸を1残基追加したトリペプチドのキモトリプシンに対する結合活性を予測しました。続いて、計算に用いた阻害剤を実際に調製し、酵素活性試験をによってその阻害活性を実測しました。そして、計算結果との比較を行い、ドッキング計算による活性予測の妥当性について検証を行いました。
(4) 溶媒摂動法を用いた生体関連分子の分子間相互作用解析
創薬研究の初期生物活性スクリーニングにおいては、酵素や受容体などの標的タンパク質のリガンド結合部位に対して特異的に結合する新規創薬シーズを創出することが重要です。酵素阻害剤の中には、酵素の触媒部分ではないところに結合してしまうものもあります(非特異性)。
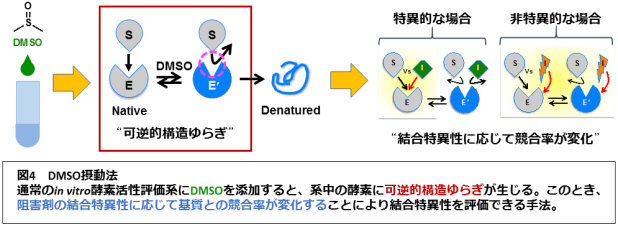
当研究室では、酵素阻害剤の結合特異性を評価するための新規手法として、「ジメチルスルホキシド(DMSO)摂動法」を開発しました。低濃度のDMSO存在下で、酵素が「可逆的な構造ゆらぎ(摂動)」の状態をとることを利用して、非特異的酵素阻害剤を簡便に見分けることができる手法です。現在、摂動効果における溶媒特異性の検討や速度論解析を行い本法の概念立証を進めるとともに、本法を用いて酵素や核内受容体などの生体関連タンパク質に結合する分子の結合特異性を評価し、生体機能の解析・制御に利用可能な新規ケミカルバイオロジーツールや創薬シーズの創出を目指して研究を行っています。
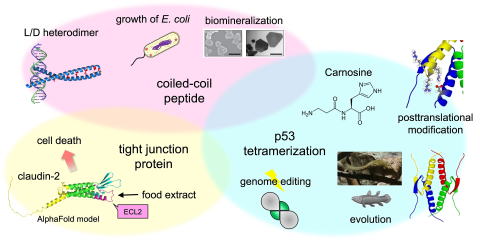
(5) 多量体形成タンパク質の機能制御機構の解明
生体内では、 多くのタンパク質が複数集まった「多量体」として働いています。 これらのタンパク質は、 わずかな構造変化や相互作用の違いによって機能が大きく変化し、
細胞の運命や病気の発症にも深く関わっています。
当研究室では、 こうした多量体形成タンパク質の相互作用と機能調節の仕組みを、 ペプチド科学・生化学・構造解析を組み合わせて研究しています。 特に、
タンパク質同士がどのように会合し、 その状態変化が細胞機能にどのような影響を与えるのかに興味を持っています。 これまで、 coiled-coilペプチドや癌抑制タンパク質p53を対象として、
多量体形成による機能制御機構の解析に取り組んできました。 これらの研究を通して、 生命現象を分子レベルで理解するとともに、 新しい細胞機能制御技術や創薬への応用につながる知見を得たいと考えています。
生体分子化学研究室
九州大学基幹教育院
自然科学実験系部門
九州大学大学院理学府化学専攻
九州大学理学部化学科
〒819-0395
福岡県福岡市西区元岡744
TEL 092-802-6025